急性ST段抬高性心肌梗死的溶栓治疗
早在19世纪,病家在尸体解剖时,发现冠状动脉内血栓形成是急性心肌梗死(acute myocardial infarction, AMI)患者的致死原因。1959年Fletcher倡导并进行心肌梗死溶栓,但由于未能很好利用挽救心肌梗死的有效时间窗口,而导致静脉溶栓的效果不佳,并认为栓塞性冠状动脉闭塞并不是AMI的主要病理生理机制。上世纪70年代后期通过大量临床和病理解剖的研究,再次认识到90%以上的AMI是由相关的冠状动脉血栓形成,造成冠脉阻塞所引起的,因此重新进行AMI的溶栓治疗研究。冠状动脉急性闭塞至心肌透壁性坏死有一时间窗, 根据动物实验研究, 这一时间窗大约为6h。在该时间窗内使冠状动脉再通,可挽救濒临坏死的缺血心肌。溶栓治疗的问世使AMI的治疗跨进了新的时代:AMI的再灌注治疗时代,其意义在于治疗的重点从被动地防治并发症,向主动地治疗导致AMI原因的转变。
一系列大规模随机双盲临床试验结果表明,AMI溶栓治疗与安慰剂对比可明显降低病死率。症状出现后越早进行溶栓治疗, 降低病死率效果越明显,但对6~12h仍有胸痛及ST段抬高的患者进行溶栓治疗仍可获益。溶栓治疗受益的机制包括挽救心肌和对梗死后心肌重塑的有利作用。
溶栓药物的药理作用和分类
凝血过程中形成的纤维蛋白,可经纤溶酶作用从精氨酸-赖氨酸键上分解成可溶性产物,使血栓溶解。溶栓药物为内源性或外源性纤溶酶原激活剂,直接或间接激活纤溶酶原,使其转化为纤溶酶,故也称纤维蛋白溶解药。溶栓药物对形成已久并已机化的血栓则难以发挥作用。目前应用于临床的溶栓药为链激酶、尿激酶、茴香酰化纤溶酶原链激酶激活剂复合物、单链尿激酶和组织型纤溶酶原激活物,这些药物的主要缺点是对纤维蛋白无特异性,诱发血栓溶解同时伴有严重出血,且半衰期短。较新纤溶药如t-PA,scu-PA有一定程度的特异性,但人体应用仍有出血并发症。近年来应用基因工程和单克隆抗体技术对溶栓药进行结构改造,高效特异的新溶栓剂已应用于临床。目前在临床上应用及正在研究开发的溶栓药物可划分为三代产品:
第一代溶栓药物包括尿激酶(urokinase,UK)和链激酶(streptokinase,SK),不具有纤维蛋白选择性。第二代有重组组织型纤溶酶原激活剂如阿替普酶(ateplase,t-PA)、阿尼普酶(anti-streplase,APSAC)等、重组单链尿激酶型纤溶酶原激活剂(sar-uplase, scu-PA)、前尿激酶(pro-urokinase, pro-UK)、重组葡激酶(recombinant staphylokinase)及其衍生物、乙酰化纤溶酶原-链激酶激活剂复合物(antistrep-lase, APSAC)等,具有纤维蛋白选择特性。
第三代溶栓药物是利用基因工程和单克隆抗体技术对第二代产品进行改造而制成的新的产品,主要特点是半衰期延长,适合静脉给药。这类药包括t-PA的变异体如瑞替普酶(reteplase,r-PA)、兰托普酶(lanetoplase,n-PA)、TNK-组织型纤溶酶原激活剂(TNK-tPA),吸血蝙蝠唾液纤溶酶原激活剂(vampire bat salivary plasminogen activator, Bat-PA),重组嵌合型溶栓药物,抗体导向溶栓药物和磁导向溶栓药物等。
溶栓治疗的适应证
1.两个或两个以上相邻导联ST段抬高(胸导联≥ 0.2 mV,肢体导联≥0.1 mV),或提示AMI病史伴左束支传导阻滞(影响ST段分析 ),起病时间 <12 h,年龄<75岁(ACC/AHA指南列为I类适应证);
2.对前壁心肌梗死、低血压(收缩压 <100 mmHg)或心率增快 (>100次/min)患者治疗意义更大;
3.ST段抬高,年龄≥75岁。对这类患者,无论是否溶栓治疗,AMI死亡的危险性均很大。尽管研究表明,对年龄≥75岁的患者溶栓治疗降低死亡率的程度低于75岁以下患者,治疗相对益处降低,但对年龄≥75岁的AMI患者溶栓治疗每1 000例患者仍可多挽救10人生命,因此,慎重权衡利弊后仍可考虑溶栓治疗(ACC/AHA指南列为Ⅱa类适应证);
4.ST段抬高,发病时间 12~24h,溶栓治疗收益不大,但在有进行性缺血性胸痛和广泛ST段抬高并经过选择的患者,仍可考虑溶栓治疗(ACC/AHA指南列为Ⅱb类适应证);
5.高危心肌梗死,就诊时收缩压>180mmHg和(或)舒张压 >110mmHg,这类患者颅内出血的危险性较大,应认真权衡溶栓治疗的益处与出血性卒中的危险性。对这些患者首先应镇痛、降低血压(如应用硝酸甘油静脉滴注、β受体阻滞剂等),将血压降至 150/90mmHg时再行溶栓治疗,但是否能降低颅内出血的危险性尚未得到证实。对这类患者若有条件应考虑直接PTCA或支架置入术(ACC/AHA指南列为Ⅱb类适应证)。虽有ST段抬高,但起病时间>24h,缺血性胸痛已消失者或仅有ST段压低者不主张溶栓治疗(ACC/AHA指南列为Ⅲ类适应证)。
溶栓治疗的禁忌证及注意事项
在考虑进行溶栓之前,应了解患者是否存在溶栓禁忌证。STEMI患者如伴有颅内出血(ICH)高风险的患者应当采用PCI而非溶栓治疗。心肺复苏过程中进行溶栓可能无效。
1.既往任何时间发生过出血性脑卒中, 1年内发生过缺血性脑卒中或脑血管事件或颅内肿瘤;
2.近期(2~4周)活动性内脏出血(月经除外);
3.可疑主动脉夹层;
4.入院时严重且未控制的高血压 (>180/110 mmHg)或慢性严重高血压病史;
5.目前正在使用治疗剂量的抗凝药[国际标准化比率(INR) 2~3],已知的出血倾向;
6.近期(2~4周)创伤史,包括头部外伤、创伤性心肺复苏或较长时间(>10 min)的心肺复苏;
7.近期(<3周)外科大手术;
8.近期(<2周)在不能压迫部位的大血管穿刺;
9.曾使用链激酶(尤其5d~2年内使用者)或对其过敏的患者,不能重复使用链激酶;
10.妊娠;
11.活动性消化性溃疡。
常用溶栓药物的剂量和用法
AMI患者被送达急诊室后,医生应迅速作出诊断并尽早给予再灌注。力争在10~20 min内完成病史采集、临床检查和记录1份18导联心电图以明确诊断。对ST段抬高的AMI患者, 应在 30 min内收住冠心病监护病房(CCU)开始溶栓,或在90 min内开始行急诊PTCA治疗。在典型临床表现和心电图ST段抬高已能确诊为AMI时,绝不能因等待血清心肌标志物检查结果而延误再灌注治
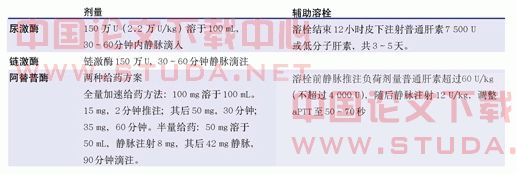
疗的时间。患者明确诊断后应该尽早用药,理想的就诊-静脉用药时间是30分钟内,但是很难达到,应该越早越好。用量和方法见表1。
表1.常用溶栓药物剂量和用法
出血并发症及处理
溶栓治疗最重要的危险是出血,尤其是颅内出血(ICH),致死率很高。降低出血并发症的关键是除外有严重出血倾向的患者(参见禁忌证)。一旦患者在开始治疗后24小时内出现神经系统状态变化,应怀疑ICH。
一旦诊断或怀疑为大出血,应当停止溶栓治疗、抗血小板和抗凝治疗,立即进行影像学检查排除ICH,应请神经科和(或)神经外科和血液学专家会诊,根据临床情况,ICH患者应当输注冻干血浆、鱼精蛋白、血小板或冷沉淀物。一旦明确脑实质出血或脑室内出血或蛛网膜下腔出血或硬膜下血肿,给予10单位冷凝蛋白质,新鲜冰冻血浆可以提供V因子和Ⅷ因子,并能增加血容量。使用普通肝素的患者,用药4小时内可给予鱼精蛋白(1 mg鱼精蛋白对抗100 U普通肝素)。如果出血时间异常,可输入6~8个单位的血小板。同时控制血压和血糖,使用甘露醇、气管内插管和高通气降低压力;考虑外科抽吸血肿治疗。
疗效评估
临床判断溶栓治疗是否有效主要根据的间接指标判定,包括:症状迅速缓解、再灌注心律失常、心肌酶学峰值前移、心电图,其中心电图和心肌损伤标志物峰值前移最重要。最为简便的方法是治疗后60~90分钟ST段抬高至少降低50%。心肌损伤标志物的峰值前移,血清CK-MB酶峰提前到发病12-18小时内,肌钙蛋白峰值提前到12小时内,提示梗死相关血管再通。溶栓成功后的2~3小时内出现再灌注心律失常,如加速性室性自主心律、房室或束支阻滞突然改善或消失、或者下壁梗死患者出现一过性窦性心动过缓、窦房阻滞伴有或不伴有低血压。患者在溶栓治疗后2小时内胸痛症状明显缓解也是再通的表现。
冠状动脉造影TIMI 2或3级血流是评估冠状动脉血流灌注的标准。但TIMI 2血流的死亡率与没再通者相比无差别,且再梗死率高,被视为无效再通。晚近的观点认为,溶栓后应早期(12小时内)常规进行冠脉造影检查,评价是否溶栓成功,而临床判断溶栓治疗失败,或只有TIMI2级血流,应进行补救性PCI。
再灌注策略的选择
STEMI早期再灌注治疗的益处以及直接经皮冠状动脉介入治疗(pPCI)优于溶栓治疗,已为大量临床试验所证实,并达成共识。STEMI死亡率和缺血心肌
的早期再灌注治疗密切相关。再灌注治疗的益处取决于缺血心肌心外膜血流的恢复时间,无论是溶栓或者是直接PCI,迅速、持久和尽早的开通梗死相关动脉是减少心肌损伤和改善预后的关键。因此,AHA/ACC STEMI治疗指南强调STEMI患者的诊断应及时准确,尽量减少(如等待心肌酶的结果等)不必要的时间延误;治疗应以尽快实施再灌注治疗为主,并辅助药物治疗;目标是实现闭塞的冠脉再通。STEMI治疗策略分两步:第一步为评估时间和危险性,评估出现症状时间,评价患者的危险程度、以及评价再灌注治疗的危险性,包括溶栓风险、转运到可熟练行pPCI导管室的时间。第二步为选择再灌注治疗方式(溶栓/pPCI):假如起病时间<3 h且PCI能及时进行,则两种治疗没有优劣之分。如发病>3小时者则宜首选PCI。尽管直接经皮冠状动脉介入治疗(pPCI)优于溶栓治疗已为大量临床试验所证实。但指南仍强调时间的重要性,及时地选择某种再灌注治疗比选择再灌注治疗方式更为重要。当有转运延迟,不能及时行PCI,进门-球囊扩张比进门-进针延迟1 h以上,进门-球囊扩张超过90 min,而进门-进针<30 min,应优先考虑溶栓治疗。对于症状出现超过3 h,进门-球囊扩张时间< 90 min,进门-球囊扩张比进门-进针< 1h,且高危STEMI患者(心源性休克,Killip3级以上),原则上应优先选择PCI。
溶栓的辅助治疗
1.阿司匹林 可增强溶栓治疗的效果,所有STEMI患者,只要没有阿司匹林过敏,立即嚼服阿司匹林300 mg,此后应当长期给予阿司匹林,每天75~160 mg。阿司匹林过敏者,应用噻吩吡啶类药物替代。
2.ADP受体拮抗剂 目前有两项研究支持AMI患者使用阿司匹林与氯吡格雷联用,强化抗血小板治疗。目前常用的ADP受体拮抗剂有氯吡格雷和噻氯匹定,但噻氯匹定粒细胞减少症和血小板减少症的发生率高于氯吡格雷。因阿司匹林过敏或胃肠道不能耐受而不能使用阿司匹林的溶栓治疗患者,建议使用氯吡格雷。
3.糖蛋白Ⅱb/Ⅲa抑制剂 糖蛋白Ⅱb/Ⅲa抑制剂与溶栓联合可提高疗效,但出血并发症增加。阿昔单抗和半量瑞替普酶或替奈普酶联合使用进行再灌注治疗可能在下列患者预防再梗死以及STEMI的其他并发症:前壁心肌梗死、年龄小于75岁,没有出血危险因素。对75岁以上的患者ICH风险明显增加,不建议药物溶栓与糖蛋白Ⅱb/Ⅲa抑制剂联合。
4.抗凝治疗 溶栓治疗的患者需要抗凝血酶治疗作为辅助治疗,应用纤维蛋白特异性的溶栓药物需要联合静脉普通肝素,如阿替普酶、瑞替普酶或替奈普酶治疗的患者。普通肝素剂量:溶栓前给予冲击量60 U/kg(最大量4 000 U),溶栓后给予每小时12 U/kg(最大量1 000 U/小时),将活化部分凝血活酶时间(aPTT)调整至50~70 s,持续48小时。低分子肝素与普通肝素比较存在用药方便,无需监测等优势,EXTRAC-TIMI25为低分子肝素与多种溶栓(链激酶、r-PA、t-PA、TNK)治疗的联合应用提供了证据,依诺肝素30 mg静脉注射,随后1 mg/kg皮下注射,每天2次:年龄大于75岁以上或肾功能不全的患者,依诺肝素减少剂量至0.75 mg/kg。
小结
虽然经皮介入治疗在冠心病应用越来越广泛,但是溶栓治疗对没有条件进行直接PCI的医院仍然是减少心肌梗死患者死亡率和改善预后的重要方法,选择恰当的适应证,减少出血并发症,在最短的时间内溶解血栓开通血管治疗仍然具有不可替代的价值。近年来介入治疗技术的快速使溶栓在心肌梗死急性期治疗中的地位受到轻视,但是溶栓治疗具有简便、、易操作的特点。即使在欧美国家,接受再灌注治疗的急性心肌梗死患者溶栓治疗与直接PCI治疗的比例相当。在目前国内经济和医疗资源分布不均衡的条件下,溶栓治疗仍然具有重要地位。溶栓辅助抗栓治疗还在不断的探索中,例如低分子肝素替代普通肝素的治疗。在临床实践中应该严格筛选适应证,的进行溶栓治疗。











