中国特有药用植物铁破锣化学成分及生物活性的研究
利用多种吸附材料和分离方法对贵州产铁破锣全草和甘肃产铁破锣根茎的乙醇提取物进行了卓有成效的分离工作,共分离得到四十个化合物,并通过经典的化学方法和各种先进的波谱学技术(包括IR,UV,1HNMR,13CNMR,DEPT,1H-1HCOSY,13C-1HCOSY,HMQC,HMBC,TOCSY,MQC-TOCSY,NOESY,EI-MS,FAB-MS和ESI-MS),鉴定了其中三十三个化合物,已鉴定的化合物中,有18个为新化合物,12个系首次从该植物中分离得到。
新化合物包括16个环菠萝蜜烷型三萜皂甙、一个齐墩果酸型三萜皂甙和一个有机酸,分别命名为:铁破锣皂甙A[BC-ll,20ε1-24ε2-epoXy-9,19-cyclolanostane-3β,16β,18,25-tetraol- 3一O-β-D-xylopyranoside],铁破锣皂甙B[BC-12,(20S*-24R*)-epoxy一9,19-cyclolanostane-3β,13β,16β,25-tetraol-3-O-β-D-xylopyranoside];铁破锣皂甙C[BC一10,(20S*-24R*)-16βacetoxy-20,24-epoxy-9,19-cyclolanostane-3β,12β,25-teriaol-3-0-β-D-xyloPyranoside];铁破锣皂甙D[BC-14,(20S*-24R*)-epoXy-9,19-cyclolanostane-3β,12β,16β,18,25-Pentaol-3-O-β-D-xylopyranoside];铁破锣皂甙E[BC-15,20εl-24ε2- epoxy-9,19-cyclolanostane-3β,12α,16β,18,25-pentaol-3一O-β-D-xylopyranoside];铁破锣皂甙F[BC-13,(20S*,24R*)-16β-acetoxy-epoXy-9,19-cyclolanostane-3β,12β,18,25-tetraol一3一O-(β-D-xylop yranoside);铁破锣皂甙G[BC一16,20ε1一24ε2一epoxy一9,19一 cyclolanostane-3β,15α,16β,18,25-pentaol-3-O-β-D-xylopyranoside];铁破锣皂甙H[gbc-23,(20S,24R)一15α,16β-diacetoxy-epoxy一9,19一cyclolanostanostane一3β,18,25一triol-3一O-β-D-xylopyranoside];铁破锣皂甙Ia[gbc-22,(20S,24S)-16β-acetoxy-18,24;20,24-diepoXy-9,19-cyclanostane-3β,15β,25-triol-3-O-β-D-xylopyranoside];铁破锣皂甙J[gbc-20,(20S,24S)-16β-acetoxy一18,24;20,24-diepoxy一9,19一cyclane-3β,25-diol-3一 O-β-D-xylopyranoside];铁破锣皂甙K[gbc-18,(20S,24S)-15α-acetoxy-16β,24;20,24-diepoXy-9,19-cyclolanostane-3β,25一diol-3-O-β-D-xylopyranoside];铁破锣皂甙L[gbc一19,15α-acetoxy一20ε1一24ε2一epoxy一9,19一cyclolanostane一3β,16β,25一triol-3-O-β-D- xylopyranoside];铁破锣皂甙M[gbc-26,(20S,24R)-15α-acetoxy-9,19-cyclolanestane-3β,6β,20,24,25-pentol-3-O-P-D-xyloPyranoside];铁破锣皂甙N[gbc-27,20ε1-24ε2-eqoxy-9,19-cyclolanostane-3β,12α,15α,16β,25-pentaol-3-o-p-D-Xylopyranoside];铁破锣皂甙o[gbc-30,20ε1-24ε2-epoxy-9,19-cycldanostane-3β,16β,18,25-tetra01-3-o-βD-glucopyranoside];铁破锣皂 甙P[gbc-31,20εl-24ε2-epoxy-9,19-cyclolanostane-3β,16β,18,25-tetraol-3-O-[β-D-glucopyrasy1一(1-6)]一β-D-glucopyranoside];铁破锣Q[gbc-33,oleanolic acid一3一o一α一L一rhamnopyranosyl一(1-4)一β-D一glucopyran03y2(1-6)-β-D-glucopyranosyl este]和铁破锣酸[BC-07,9-苯基一2E,4E,6E,8E-壬-四烯酸]。
已知化合物包括3个三萜,即:蒲公英萜酮(BC-01),蒲公英萜醇(BC-02),表木栓醇(BC-03);2个甾醇,即:E-24ξ-ethyl-ch01est-22一en一3α一ol(BC-04),β一谷甾醇(BC-05);3个有机酸,即:香草酸(BC-06),阿魏酸(gbc-17),硬脂酸(gbc032);4个环菠萝蜜烷型三萜皂甙,即:升麻醇-3-o-β-D-吡喃木糖 甙(gbc-08),25-脱水升麻醇-3-O-β-D-吡喃木糖 甙(gbc-09),beesideI(gbc-21))beesioside(Ⅲ(gbc-25);2个齐墩果酸型三萜多糖皂 甙,即:铁破锣皂甙R[oleanolic acid一3一o一α一L-rhamnopyranosyl(1-2)一α一L一rhaminopyranosyl一(1-2)一。-L-arabinopyranosyl-(1-2)-α-L-arabinoyranosyl-28-O-α-L-rhamnopyranosyl-(1-4)-β-D-glucopyranosyl(1-6)-β-D-glucopyranosyl ester];铁破锣皂 甙S[gbc-35,oleanolicacid一3一o-β-D-glucoPyranosyl(1-3)一α一L-arabinoPyranosyl-28一o一α一L一rhamoopyranosy1一(1-4)一β-D-g1ucoPyranosyl(1-6)一β-D-g1ucopyranosyl ester3和胡萝卜甙(gbc一24)。
对铁破锣中分离鉴定的部分单体化合物进行了初步的生物活性筛选试验。受体结合试验表明部分单体化合物对三种受体(5-HT受体、钙通道和GABA受体)具有一定的拮抗活性。在较低浓度(5μg/ml)时,化合物gbc021-23和gbc-25对淋巴细胞增殖具有显著的促进作用;在一定浓度范围20-100μg/ml)时,化合物BC-11、BC-12和BC-14对GLC-82细胞株显示一定的抗肿瘤活性并且成一定的量效关系。首次发现两个结构较为独特的化合物,显示出了较好的药活性,有一定的应用和开发前景。这两个化合物是:铁破锣皂 甙M(gbc-26)在低浓度(10μh/mt)时对钙通道的拮抗活性达79.55%,是一种钙拮抗剂,有望在防治心血管系统疾病方面有所突破。铁破锣皂甙K(gbc-18)在小鼠体内试验可明显抑制由ConA诱导的T细胞增殖,具有免疫抑制作用,是一种免疫抑制剂;鸡胚尿囊膜试验还显示铁破锣皂 甙K还有抑制微血管生成方面的活性(20μg/ml);其作用机理值得深入研究。这项研究工作为寻找开发新药的先导化合物及进一步开发和利用铁破锣这一丰富的药用植物资源奠定了坚实的基础。
关键词 铁破锣属 铁破锣 化学成分 环菠萝蜜烷型三萜皂 甙 齐墩果酸型三萜皂 甙铁破锣皂 甙A-Q 铁破锣酸 药理活性 钙离子受体拮抗活性 免疫抑制活性 抑制血管生成活性化学成分与民间疗效关系
结果与讨论
一、结构解析举例
1.铁破锣皂甙B(beesioside B,BC-12)的结构测定
化合物BC-12,白色无定型粉末,mp.250-252℃(CHCl3-MeOH),[α]D20十13.6。(CHCl3 MeOHl:1,c,0.11),Liebermann-Burchard反应阳性,Molish反应阳性,薄层水解检识有木糖(BAW4:1:1)。FAB-MS显示m/z 623[M十H]+,结合1H和13CNMR谱数据推测其分子式为C35H58O9,不饱和度为7。
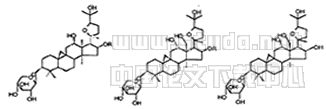
BC-01 BC-02 BC-03 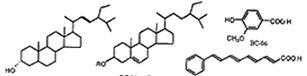
BC-04 BC-05 R=H *BC-07
gbc-24 R=Gic 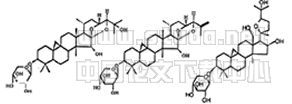
gbc-08 bgc-09 *BC-14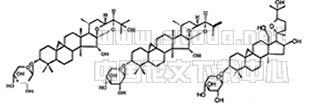
*BC-10 R=COCH3 *BC-13 R=COCH3 *BC-14
*BC-10 R=H *BC-13 R=H
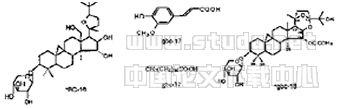
*BC-16 gbc-32 *gbc-18 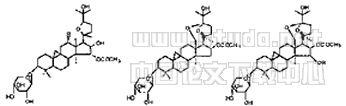
*gbc-19 R=H *gbc-20 gbc-21 R=COCH3
gbc-25 R=OH *gbc-22 R=H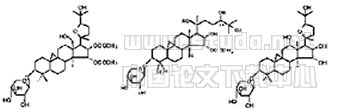
*gbc-23 gbc-26 *gbc-27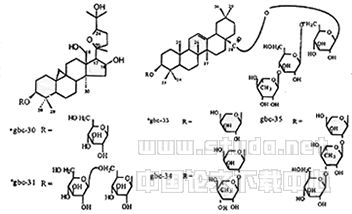
Fig 1 Structures chemical constituents isolated from
beesia calthaefolia (Maxim.)Ulhr.
IR谱在3600-3100及1045,1065cm-1出现强吸收,示甙类化合物;FAB-MS和EI-MS出现基峰m/z143(离子a),及失水峰m/z125(离子b),提示分子中存在部分结构A(25-羟基-20,24-环氧残基),这是ocotillone型三萜的典型特征;1HNMR谱中δ3.93(1H,t,J=8.0HZ可以归属A结构中的H-24,其13CHMR谱数据同beesiosideⅢ比较一致,证明A部分结构的存在。
lHNMR谱高场区显示一对AB系统质子的信号[δ0.35(1H,D,J=3.6Hz,19-H),o,58(1H, d,J=3.6Hz,19-H)],七个叔甲基质子的单峰信号[δ0294,1.00,1.31,1.36,1.59,1.68(2× CH3)],提示该化合物的骨架为环菠萝蜜烷型三萜。糖的端基氢信号出现在δ 4.84(1H,d,J=7.6Hz),说明甙键为β构型。低场区除了木糖质子和H-24信号外,还显示2个连氧碳上的质子信号[δ4.81(1H,m,Hz),4.14(1H,m,同H-3'重叠,Hx)]。
13CNMR谱共显示35个碳信号。一组碳信号[δ107.45,75.53,78.52,71.26,67.05]可归属为木糖的C-1~C-5。低场区除了C-3和A部分结构碳信号外,还显示2个连氧碳信号[δ72.07,73.10]。
1HNMR谱中17位氢出现在δ2.76(1H,d,J=8.4Hz),考虑化合物的不饱合度,说明16位有羟基取代;1H-1H COSY谱中δ4.8l(Ha,H-16)与δ2.76(H-17)相关,还与δ2.15(1H,m,H-15)和δ1.93(1H,m,H-15)两个氢相关13C-HCOSY谱中,δ72.07与84.81(Ha,H-16)相关5根据偶合常数(J16,17)大小可判断16经基与17位侧链处于顺式位置,因此确定16位经基为β构型;NOESY谱中,H-16α与H-17α相关,证明了上述结论。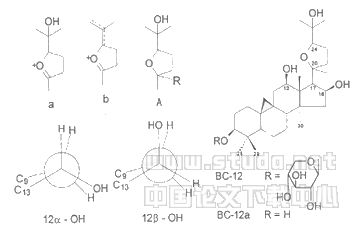
Fig 2 Structure of BC-12(beesioside B)
13CNMR谱中,C-18出现在高场区[δ14.05],提示12位有羟基取代,这是因为C-18处在12位羟基的γ位引起高场位移所致。13C-1HCOSY谱中,δ73.10(C-12)与δ4.14(Hx,H-12)相关;1H-1H COSY谱中δ4.14(Hx,H-12)与ll位两个氢δ2.55(1H,dd,Jl=15.4,J2=8.8Hz,H-11α),1.42(1H,dd,Jl=15.4,J2<3.0Hz,H-11β=相关;HMBC谱中,H-18和C-12远程相关,证明了上述结论。
化合物BC-12经异相酸水解得BC-12a,EI-MS亦出现基峰m/z143(离子a),及失水峰m/z125(离子b),提示分子中存在A部分结构,1HNMR谱中δ3.94(1H,t,J=7.4Hz)可以归属A结构中的H-24,其13CNMR谱数据同beesiosideⅢ比较一致,证明A部分结构的存在。1HNMR谱显示环丙烷质子信号[δ0.39(1H,dd,J=3.5Hz,19-H),0.63(1H,dd,J=3.5Hz,19-H)]七个叔甲基质子的单峰信号[δ0.96,1,03,1.20,1.35,l.58,1.68,1.70],及δ2.76(1H,d,J=8.3Hz,H-17),3.49(1H,dd,J=11.4,4.3Hz,H-3α),4,82(1H,q-1ike,J=7.4Hz,H-16);另外还显示一对ABX系统质子信号[δ2.58(1H,dd,J=15.4,8.9Hz,H-11),1.43(1H,dd,J=15.4,2.7Hz,H-11)和4.16(1H,dd,J=8.9,2.7Hz,H-12)。13CNMR谱共显示30个碳信号;其中c-3向高场移至δ77.98。
12位经基的构型是通过比较H-12和H2-11之间的偶合常数确定的。SakuraiN等用X光衍射的方法测定了beesiosideⅡ甙元的双乙酰化物的结构,其c(9)-c(11)-c(12)-c(13)间的拓扑角为-14.4。,若12-OH为α构型,则H-12和H2-11之间的偶合常数J1约为8Hz,J2>4Hz;若12-OH为β构型,则H-12和H2-11之间的偶合常数Jl约为8Hz,J2<3Hz(Fig,2)。在化合物BC-12a中H-12和H2-11之间的偶合常数Jl=8.9,J2=2.7Hz;化合物BC-12中H-12和H2-ll之间的偶合常数Jl=8.8,J2<3.0Hz,因此确定12-OH为β构型。NOESY谱中,H-12α/Me-30/H-17α之间存在相关,亦支持这一结论。
BC-12的1HNMR谱中3位氢出现在δ3.47(1H,dd,J=11.7,4.2Hz),根据其裂分方式和偶合常数大小可判断3位氢为α构型;NOESY谱中H-28和H-3α相关,也支持上述结构;与化合物BC-12a比较其C-3位苷化位移值(低场位移10.48ppm),确定木糖连在C-3位。HMBC谱 中H-1'(δ4.84)和C-3(δ88.46)远程相关,证明了这一结论。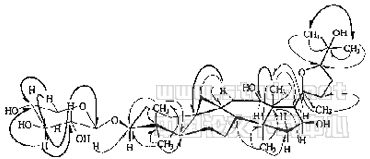
Key correlations observed from HNBC of BC-12
Significant correlation observed from NOESY of BC-12
Fig 3 HMBC and NOESY of bc-12
BC一12的NOESY谱中,H-16α/H-α/Me-21、Me-21.H-22α/H-23α/H-24α、H-22α/H-22β、H-23α/H-23β、H-22β/H-23β、H-24α/Me-26/Me-27之间检测到NOE相关信号(Fig,3),因此A部分结构的构型确定为20S*,24R*。
Tab1.1HNMR(500MHz)and13CNMR(125MHz)Spectral Data of BC-12(beesioside B),BC-12a and gbc-26(beesioside M)in pyridine-d5
Position | BC-12(beesioside) | δ13C | BC-12a | Beesioside M(gbc-26Δ) | δ13C |
1 | 1.28m;1.54m 1.30m | 32.24 | 32.47 25.78 | 1.21m;1.54m 1.30m | 32.40 |
11-α | 2.55dd(15,4,8.8) | 37.97 | 38.04 73.16 72.08 86.38 | #,# 1.75m;1.85m
4.69dd(8.3,3.5) | 26.05 34.23 76.43 |
21 | 1.68**s 2.16m 2.87dt 1.91m 2.27m 3.93t(8.0) 1.59s 1.36s 1.31s 1.00s 0.94s | 28.99 25.82* 82.97 | 29.00 26.22* 82.96 | 1.47s 2.15m;2.02m 3.76br.d(9.0) 1.50s | 26.00* 27.16 80.34 |
COCH3 |
4.84d(7.6) |
107.45 | 2.03s 4.82d(7.4) | 21.29 |
结合 1H-1HCOSY,13C-1HCOSY,NOESY和HMBC光谱,所有的碳氢信号都得以归属(Tab.1,Fig,3,)。综合以上证据,测定该化合物BC-12为(20S*一24R*)-epoxy-9,19-cyclolanostane-3β,12β,16β,25-tetraol-3-O-β-D-xylopyranoside,命名为铁破锣皂甙B(beeside B)
2.铁破锣皂甙M(beesioside M,gbc-26)的结构测定
化合物gbc-26,白色无定型粉末,mp。274-276℃(CHCL3-MeOH,c,[α]D20十2.6。(MeOH,c,0.12),Liebermann-Burchard反应阳性,Molish反应阳性、薄层水解检识有木糖。FAB-MS显示 m/z683[M十H]+,结合1HH和13CNMR谱数据推测其分子式为C37H62O11,不饱和度为7。
IR谱在3600-3100及1040,1090cm-1出现强吸收,示甙类化合物;在1720,1260cm-1显示强吸收带,提示分子结构中含乙酰基。1H和13CNMR谱提示该化合物为9,19环菠萝密烷型三花单糖甙,含有一个乙酰基[δH2.03(3H,s),δc17l.563(Tab.1)。
1HNMR谱高场区显示一对AB系统质子的信号[δ0.29(1H,d、J=3.9Hz,19-H),0.50(1H,d,J=3.9Hz,19-H)],七个叔甲基质子的单峰信号[δ1.01,1.08,l.28,1.47,1.50,1.53,1,833,还显示一组木糖的5个质子信号[δ3.69(1H,t,J=10.6Hz,5'-H),3.97(1H,t,J=8.0Hz,2'-H),4.10(1H,t,J=8.6Hz,3'一H),4.15(1H,m,4'一H),4.32(1H,dd,J=11.2,5.1Hz,5'一H),4.82(1H,d,J=7.4Hz:,1'-H)];根据端基氢的偶合常数可判断贰键为β构型。
1HNMR谱低场区显示一个ABX系统连氧碳上的质子信[δ5.56(1H,d,J=3.5Hz,Ha)4.69(1H,dd,J=8.3,3.5Hz,Hb),2.29(1H,d,J=8.3Hz,Hx)]。HMQC谱中,Ha(H-15),Hb(H-16)和Hx(H-17)三质子信号分别与碳谱中δ90.75(C-15),79.94(C-16)和54.09(C-17)相先考虑到Ha(H-15)化学位移处于较低场,推测15位连有乙酰氧基,该化合物具有部分结构B(Fig,4)。
13CNMR谱共显示37个碳信号;一组碳信号[δ107.39,75.42,78.42,71.19,66.98]可归属为木糖的C-1~C-5。δ88.49可归属为C-3。该化合物的不饱和度为7,扣除9,19环菠萝蜜烷型A-D环骨架、一个糖环和一个乙酰基引起的不饱和度,分子中不再有其它环系。因此17位应连有一个8碳开环侧链。13CNMR谱低场区除了C-3、C-15,C-16和木糖碳信号外,还显示3个连氧碳信号[δ80.34,76.43,72.81],说明分子中还有3个羟基。
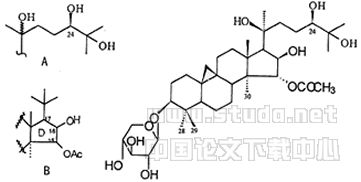
Fig 4 Structure of gbc-26 (beesiosede M)
1HNMR谱中甲基信号均为单峰,说明有一羟基位于25位,连氧碳信号δ72.81可归属为C-25。H-17只与H-16偶合呈双峰,提示C-20为季碳,说明有一羟基连在20位碳原子上,连氧碳信号δ76.43可归属为C-20。从生源上推测,另一羟基位于24位,1HNMR谱中低场区出现一质子信号δ3,76(1H,br,d,J=9,0Hz,H-24),HMQC谱中,H-24与δ80.34相关HMBC谱中,H-27与C-24远程相关,H-24与C-23,C-22远程相关,H-21与C-17,C-20,C-21远程相关(Fig.5),证明了3个羟基位于C-20、(C24和C-25位。FAB-MS出现基峰m/143(100),107,可解释为17位侧链部分分别失去一分子和三分子水所致。以上证据说明分子中存在部分结构A。
1HNMR谱中3位氢出现在δ3.47(1H,dd,J=11.6,4.1Hz),根据其偶合常数和裂分方式可判断3位氢为α构型。HMBC谱中的,δ4.82(H-1')与δ88.49(C-3)相关证明木糖连在C-3位。
结合HMQC,HMBC和与相关化合物beessioside L(gbc-19)比较,所有碳信号和大部分氢信号都得以归属(Tab.1);因此该化合物的平面结构得以确定(Fig.4)。
C-15,16和17的立体化学是通过研究1H-1H偶合常数(J15,16=3.5,J16,17=8.3Hz)确定的。H-16和H-17之间偶合常数为8.3Hz,说明16位羟基与17位侧链处于顺式位置,即16位羟基为β构型;H-15和H-16之间偶合常数为3.5Hz,说明15位乙酰基α构型(若15位取代基为β构型,则J15,16=9Hz)。
天然界中,17位含八碳开环侧链的四环三萜类化合物在20,24,25位同时具有3个羟基取代的化合物并不多见,从紫云英属(Astragalus)中曾报道过侧链含24,25双羟基取代的四环三萜皂甙,Hirotani M等认为根据C-24的化学位移值可以判断C-24的绝对构型,24R构型时,C-24化学位移出现在δ79.7-80.5;24S构型时,C-24化学位移出现在δ77.1-77.3;同时报道了3个24S构型的环菠萝蜜烷型四环三萜皂甙类化合物,其C-24化学位移均出现在肝7.1-77.3。Inada A等报道了3个24R构型的环菠萝蜜烷型四环三花类化合物,其C-24化学位移均出现在δ79.7-80.0。化合物gbc-26中C-24化学位移值在δ80.35,因此推测其C-24的构型为24R。
在人参属植物中曾发现C-20含羟基取代的Ⅲ型化合物,报道,12-OH取代的化合物,20-OH与12-OH存在形成氢键的可能,此时20R或20S构型的化合物,其C-20的化学位移才有较大差别,可以根据C-20的化学位移判断20位的构型;但12位无羟基取代时,其C-20的化学位移并无显著差异。化合物gbc-26的1HNMR谱中有一甲基单峰出现在较低场δ1.83,根据HMBC谱(fig.5)应归属为18-CH3,与化合物gbc-19比较,其化学位移明显向低场位移,这显然是受到C-20羟基空间电负性作用的影响所致,说明20-OH与18-CH3处于δ位,因此20-OH确定为β构型,从推断C-20的绝对构型为S。
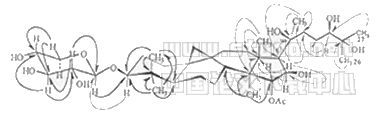
Fig.5 Significant correlations observed from HMBC of gbc-26
综合上述分析,测定化合物gbc-26的结构为(20S,24R)-15。-acetoxy-9,19- cyclolanostane-3β,l6β,20,24、25-pentaol-3-O-β-D-xylopyranoside,命名为铁破锣皂甙M(beesioside M)。
二、铁破锣化学成分与民间疗效关系问题的讨论及其应用前景问题的展望
铁破锣分布于我国南北各省,其根茎或全草药用,在民间有广泛的用药基础,具有清热解毒,凉血,活血,消肿,镇痛,散风寒的功效。民间用来风寒感冒,风湿关节痛,红白痢疾,咽喉肿疼,头痛,牙痛等病,外敷治疗疮疗和毒蛇咬伤等。因此,从药的观点来看其民间疗效体现在三方面,即:解热镇痛抗炎作用、对心血管系统的作用、解毒及潜在的抗肿瘤作用。
我们通过对铁破锣进行系统的化学成分研究,从中分离出大致三种类型的化学成分,即:三萜及甾醇类、有机酸类和三萜皂甙类;全草中三类成分均有,根茎中只含后两类成分;无论全草或根茎,其三萜皂甙类化学成分都占绝对优势,是铁破锣的主要成分。
文献报道,蒲公英萜醇(taraxerol)具有抗溃疡及抗胃酸分泌的作用。表木栓醇(epifriedlinol),有抗炎作用;腹腔注射30mg/kg,对交叉莱胶引起的大鼠足趾水肿可抑制50.1%。香草酸(vanillicacid)具有抗菌和抗真菌作用,体外实验还显示抗炎活性。阿魏酸(ferulic acid)具有抗菌、抗真菌、抗肝(细胞毒)、抗雌激素、抗肿瘤和抗有丝分裂等活性;体外可激活吞噬作用,还能抗氧化和清除自由基,保护膜脂体不受氧化。我们从铁破锣中分离得到的以上化合物揭示了其解热镇痛抗炎等方面的作用。
我们对铁破锣中含量较高的三萜皂甙类化学成分进行了精细的分离工作,结果显示大部分单糖甙及双糖甙均具有环菠萝蜜烷型四环三萜母核,而多糖甙则具有齐墩果酸型母核。
我们对部分环菠萝蜜烷型皂甙类单体化合物进行了初步的活性筛选试验,结果显示其对 5-羟色胺受体有一定的抑制活性,5-经色肤是一种重要的炎症介质,提示此类化合物抗炎镇痛等方面的作用;部分单体化合物对钙离子受体显示了相对较强的拮抗活性,钙离子与cAMP共同组成第二信使,说明此类化合物在心血管)如扩血管、降压、促智等)方面的作用。对此类化合物的抗肿瘤实验结果表明多数单体化合物在低浓度(5μg/ml)时几乎不显示细胞毒作用,在一定浓度范围(20-100μg/ml)对某此瘤株显示一定的细胞毒活性。我们从中得到的升麻醇木糖甙(Cimigenolxyloside),文献报道此化合物在较大剂量(300mg/kg,p,o,)时,能有效的抑制小鼠CCL4诱导引导起的肝损伤。揭示了铁破锣在治疗疮疖和解毒方面的作用。
铁破锣中齐墩果酸型三萜多糖皂甙的分出,体现出铁破锣在升麻族中的个性,已报道此种骨架的皂甙具有广泛的药理学活性涉及到增强机体免疫力、镇痛、降血脂、降血糖、降血压、保肝、抗癌及激素样作用等。日本学者曾报道过几个与铁破锣皂甙Q-S结构较为相近的化合物。这几个化合物可防止CCl4诱导引起的肝损伤,抑制天冬氨酸转氨酶和丙氨酸转氨酶的活性;这提示铁破锣中齐墩果酸型三萜多糖皂甙可能与其解毒方面作用有关连。
在对单体化合物的筛选过程中,我们发现铁破锣皂甙M(gbc-26)在低浓度(10μg/ml)时对钙通道的拮抗活性达79.55%,是一种钙拮抗剂,有望在防治心血管系统疾病方面有一定的前景;从化学结构上看,此化合物在17位含有一个八碳开环侧链,且有天然产物中不太多见的20,24,25三羟基取代,比20,24环氧结构的化合物活性强的多,这一现象提示侧链开环的化合物对钙通道具有更高的拮抗活性,20,24,25三羟基可能与活性有关;这一初步的构效关系理论为寻找开发新药的先导化合物提供了思路。
另一个结构上较为新颖的化合物,铁破锣皂甙K(gbc-18)在小鼠体内试验可明显抑制由 ConA诱导的T细胞增殖,具有免疫抑制作用,是一种免疫抑制剂;另外铁破锣皂甙K还有抑制微血管生成方面的活性(20μg/ml);化学结构上看,此化合物含有20,24;16,24双环氧的缩酮结构,其作用机理值得深入研究。
天然产物在新药研制和人类卫生保健中占有重要地位,天然产物是大在漫长地进化过程中形成的,凝结了朴素的思想,其疗效肯定,已成为食品、药品、化妆品等研制与开发的广泛的物质基础。我们通过对铁破锣系统的研究工作为寻找开发新药的先导化合物及进一步开发和利用铁破锣这一丰富的药用植物资源奠定了坚实的基础。
实验部分
一、 仪器药品(略)
二、 提取分离(略)
三、 药理活性研究
1. 受体结合试验
(1)材料及模型代号(方法略)
a 样品来源:从铁破锣中分离得到的单体化合物。
B 模型代号:SHT5LSC、CA+channelLSC、CABALSC、M1受体、A1受体
样品代号 | SHT5LSC | Ca+channelLSC | CABALSC | M1受体 | A1受体 |
BC-11 | 29.16 | 48.48 | 33.26 | 0 | 42.32 |
(2)模型说明
模开代号 | 分子靶点 | 阳性对照 | 测 试 指 标 |
5HT5LSC | 5-HT受体5亚型 | 5-羟色胺 | 样品对3H-LSD同该受体结合的抑制率 |
结论:5-羟色胺是一种重要的炎症介质;钙在维持心血管细胞功能方面极为重要,与cAMP共同起第二信使作用;GABA是一种抑制性神经递质;以上多数单体化合物对三种受体具有一定的拮抗活性。其中化合物gbc-26在低浓度时对钙通道的拮抗活性达79.55%,是一种钙拮抗剂,有望在心血管系统疾病方面有一定前景。
2. 体外抗肿瘤试验(1)实验材料及模型代号(方法略):
a 样品来源:从铁破锣中分离得到的单体化合物,DMSO溶解配置样品。
b 模型代号:Bel-7402,kb,GLC-82细胞株淋巴细胞。
样品代号 | 浓度(μg/ml) | Bel—7402抑制率% | KB抑制率% | 淋巴细胞增殖率% |
BC-11 | 5 | 0 | 0 | 7.8 |
Tab.4 部分化合物在不同浓度下对BLC-82细胞的抑制率**
样品代号 | 浓度(20μg/ml) | 浓度(50μg/ml) | 浓度(100μg/ml) |
BC—11 | 30.9 | 35.6 | 49.8 |
结论:以上单体化合物在低浓度(50μg/ml)时几乎不显示抗肿瘤活性,但gbc-21~23和gbc-25对淋巴细胞增殖具有显著的促进作用。在较高浓度(20μg/ml,此浓度下仍有评价意义)时,化合物BC-11、BC-12和BC-14对GLC-82细胞侏显示一定的抗肿瘤活性,并且成一定的量效关系。
3. 体内实验对小鼠免疫功能的影响
(1)验材料、仪器(略)
(2)实验方法
a 小鼠脾细胞悬液的制备:将小鼠拉颈处死,用75%乙醇浸泡1-2分钟,在超净台内无菌取脾,置盛有Hank's液的平皿中于钢网上剪碎用针芯轻轻研磨,即成单细胞悬液。离心10分钟(1000rpm),弃上清液后洗两次,进行细胞记数,细胞觉淀用c-RPMI1640培养液调至1×107/ml浓度。
b MTT法淋巴细胞增殖反应实验
新鲜分离的1×107/ml小鼠脾细胞悬液加入96孔细胞培养板中,每空加入100μl,再根据实验设计加入刺激剂(ConA)100μl/孔,每个样品设三个平行孔并设对照孔(仅加c-1640),每孔总体积200μl,然后将培养板置于37。C的5%CO2培养箱中培养48小时。取出培养板,每孔吸弃上清液100μl,各孔加5mg/mlMTT10μl,继续培养4小时。取出培养板,各孔加10%SDS裂解液100μl,放培养箱中过夜,于570nm处酶标仪比色测定OD值,并转化值OD值。
组别 | 给药量(ng) | 转化值(OD±SD) | ΔOD |
| 空白对照 | — | 0.617 | — |
| BC-12 | 10 | 0.603±0.023 | -0.014 |
| 50 | 0.717±0.267 | 0.100 | |
| BC-14 | 10 | 0.539±0.141 | -0.122 |
| 50 | 0.630±0.187 | 0.013 | |
| gbc-18 | 10 | 0.285±0.008 | -0.368 |
| 50 | 0.323±0.033 | -0.294 | |
| gbc-19 | 10 | 0.730±0.063 | 0.113 |
| 50 | 0.702±0.016 | 0.085 | |
| 空白对照 | — | 0.581 | — |
| gbc-21 | 10 | 0.998±0.145 | 0.417 |
| 50 | 0.804±0.234 | 0.223 |
结论:体内实验表明,单体化合物gbc-18在小鼠体内给药时可明显抑制由ConA诱导的T细胞增殖,具有免疫抑制作用,是一种免疫抑制剂。单体化合物gbc-21在小鼠体内给药时可明显促进由ConA诱导的T细胞增殖,具有免疫增强作用。
4.鸡胚尿囊膜(CAM)试验
(1)实验目的:观察单体化合物(gbc-18)对新生血管生成的影响
(2)实验材料及实验方法:
a.样品来源:从铁破锣中分离得到的单体化合物(gbc-18)。
b.种蛋来源:购自国防大学。
c.药品制备及对照:o.5mg单体化合物(gbc-18)溶于75%乙醇37.5μl,再加生理盐水至总体积100μl,即得5mg/m1药液,等体积混合溶媒做阴性对照,1:3氢考肝素混合液做阳性对照。
d.鸡蛋孵化:将种蛋置恒温、恒湿(37℃,60%)孵化箱中孵化,72小时后打破蛋壳入100mm平皿中继续孵化72小时之后加药(见下)。
e.加药:将上述5mg/ml浓度药液稀释至20μg/ml,溶媒对照做同样稀释后加在自制约2mm玻璃纤维滤纸片上,每片加药液3μl(药片),将药片分别放在鸡胚尿囊膜血管分枝处,24小时后解剖显微镜下观察该处血管变化。
(3)实验结果:
本实验结果:加化全物gbc-18的药片处,血管发生自溶现象,无新生血管形成;溶媒对照药片处血管无变化;氢考-肝素药片处血管出现空白,无新生血管形成。
(4)结果分析与结论:
肿瘤细胞分裂增生迅速,肿瘤的生长伴随着微循环方面的血管增生,其营养成分是靠毛细血管运输的;鸡胚尿囊腊(CAM)试验旨在检验药品对微循环方面的影响,从这一角度评价和筛选抗肿瘤药物。本实验结果表明,单体化合物gbc-18有抑制微血管生成方面的活性;其作用机理有待于进一步研究。











