HBV M 定量与HBV DNA检测的相关性研究
作者:冯 瑶1,张乐之2,吴淑梅2,王智华3,方超平2
【摘要】 目的 探讨HBV M与HBV DNA检测的相关性及定量检测HBV M的临床应用价值。方法 荧光定量PCR定量检测HBV DNA,时间分辨荧光免疫分析法定量检测HBV M。结果 三组患者血清中HBeAg检出率差异有显著性(P<0.01)。HBV DNA在102~103 copy/μl时与HBV M无相关性(P>0.05);HBV DNA≥104copy/μl时与HBsAg及HBeAg成正相关(P<0.01),与HBsAb、HBeAb及HBcAb无相关性(P>0.05);三组患者中HBsAg与HBsAb有相关性(P<0.01), HBeAg与HBeAb在HBV DNA≤107 copy/μl时成负相关(P<0.01),HBV DNA≥107copy/μl时无相关性(P>0.05)。结论 HBsAg和HBeAg抗原可作为监测HBV感染和复制的量化指标。动态监测HBV M的量能够反映机体对病毒感染的免疫反应情况,可作为观察临床病程、疗效的依据。
【关键词】 乙型肝炎病毒标志物;乙型肝炎病毒DNA;荧光定量PCR;时间分辨荧光免疫测定法
【Abstract】 Objective To investigate the relationship between HBV DNA concentration and serological markers’(HBV M)concentration, and to explore the significance of qualifing the HBV serological markers, concentration.Methods TRFIA was used to detect the concentration of HBV M, fluorescence-quantitative PCR was used to qualify the HBV DNA concentration. Results In three group patients,the positive rates of HBeAg were significant difference (P<0.01).In I group (HBV DNA 102~103 copy/μl),the HBV DNA is no related to HBV M (P>0.05). When the HBV DNA ≥104copy/μl,the HBV DNA is closely related to HBsAg and HBeAg (P<0.01),while the HBV DNA is no related to HBeAb and HBcAb(P>0.05).In three group patients HBsAg is related to HBsAb(P<0.01).When the HBV DNA ≤107copy/μl HBeAg is related to HBeAb(P<0.01).When the HBV DNA≥104copy/μl HBeAg is no related to HBeAb(P>0.05).Conclusion TRFIA is a sensitive method for HBV M quantification, which can monitor patient’s condition and therapeutic efficacy, and suggest the prognosis of chronic hepatitis. HBsAg and HBeAg can be monitor HBV infection and reproduce.
【Key words】 HBV M;HBV DNA;fluorescence-quantitative;PCR;TRFIA
随着全自动荧光定量PCR仪的问世,HBV DNA定量检测在确诊HBV感染中的地位更加巩固,但因其操作环境和技术要求较高,价格比较昂贵等原因使其应用受到了一定限制。本文采用时间分辨荧光免疫分析法(TRFIA)定量检测HBV阳性患者血清HBV M,探讨定量检测HBV M与HBV DNA的相关性,旨在寻找一种确诊HBV感染的简便易行的方法,现报告如下。
1 对象与方法
1.1 标本来源 选自门诊及住院患者血清HBV DNA阳性(HBV DNA≥5×102copy/μl)标本66例,其中男40例,女26例,年龄15~64岁。收集血清标本置-20℃冷冻保存待检。
1.2 仪器 德国ROCHE公司Lightcycler荧光定量PCR仪;上海新波ANYTEST2000时间分辨荧光分析仪。
1.3 检测方法试剂 HBV DNA 采用FQ-PCR定量检测,试剂选用深圳匹基公司生产乙肝病毒(HBV)核酸扩增(PCR)荧光检测试剂盒;HBV M检测采用时间分辨荧光免疫分析法,试剂选用上海新波公司生产的乙肝血清标志物定量检测试剂盒;以上实验均严格按说明书操作。
1.4 阳性结果判断标准 HBV DNA>5×102copy/μl;HBsAg>0.2ng/ml;HBsAb>10mIU/ml;HBeAg>0.03NCU/ml;HBeAb>0.85NCU/ml;HBcAb>0.095NCU/ml者判为阳性。
1.5 统计学分析 计数资料采用χ2检验,相关性用相关检验分析,成对双样本均值分析用t检验。
2 结果
按HBV DNA拷贝数将待测标本分三组:Ⅰ组20例:HBV DNA拷贝在102~103copy/μl;Ⅱ组26例:HBV DNA拷贝在104~106 copy/μl;Ⅲ组20例:HBV DNA拷贝≥107 copy/μl。因部分标本HBV M浓度过低无值,故采用HBV M荧光数进行统计处理。
2.1 三组中HBV M阳性检出率 见表1。
2.2 HBV DNA与HBV M各项数值间相关系数r值及P值 见表2。
3 讨论
本文应用TRFIA法定量检测HBV DNA阳性血清中HBV M,结果表明HBsAg和HBeAg均有较高的阳性率(见表1),其中HBeAg在不同DNA拷贝组中氧性率差异有显著性(P<0.01)。同时随HBV DNA拷贝升高HBsAg、HBeAg和HBcAb呈升高趋势,HBeAb呈下降趋势,HBsAb变化趋势不明显,且二个抗原在不同DNA拷贝组中的值差异有显著性(P<0.01),其余项目差异无显著性(P>0.05),支持Theilmann[1]、Neurath[2]等认为HBsAg、肝内HBcAg及HBeAg滴度成正相关。说明以上HBV抗原在数量上与HBV DNA拷贝数有良好相关性,可望作为监测HBV感染和复制的量化指标。
表1 三组患者血清HBV M阳性率(%)
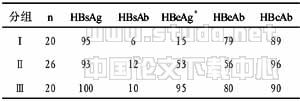
注:χ2检验,*P<0.01
表2 HBV DNA与HBV M 各项间相关系数及P值
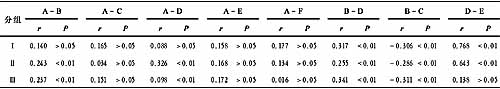
注:A-HBV DNA;B—HBsAg;C—HBsAb;D—HBeAg;E—HBeAb;F—HBcAb
由表2可以看出在HBV DNA<104 copy/μl时与HBV M无相关性(P>0.05)。HBV DNA≥104 copy/μl时,与HBsAg和HBeAg成正相关(P<0.01); 与HBeAb浓度成负相关(P<0.01);HBsAb及HBcAb无相关性(P>0.05)。这可能是因为病毒低水平复制时机体存在转换不稳定现象,此时依靠定量检测HBV M不能说明病毒的复制水平。在病毒复制活跃时,可以依靠定量检测HBV M来判断病毒复制水平。
由表2可知HBsAg与HBsAb均成负相关,在HBV DNA拷贝数<107copy/μl时HBeAg与HBeAb荧光数成正相关,与浓度成负相关,提示HBV的感染及复制情况与机体对HBV的免疫反应状态具有一致性,即病毒复制越活跃机体免疫应答水平越高。同时说明应用TRFIA法定量检测HBV M,可以监测处于转化期患者的病情和效果,较早地提示肝炎慢性化进程;定量分析HBsAg与HBsAb浓度变化,可以预示急性乙肝是否处于恢复期,定量分析HBeAg与HBeAb的浓度变化可以反映HBeAg向HBeAb转换的时期[3~5]。
综上所述,PCR法检测HBV病毒本身(DNA),能够准确、灵敏地反映HBV的感染和治疗恢复情况,但因其实验条件要求严格、操作繁琐,不便于广泛开展。我们采用TRFIA法定量检测HBV M,不但可以定量反映病毒感染及复制水平,还可通过动态监测抗原抗体量来反映机体对病毒感染的免疫反应情况,为观察临床病程、疗效提供可靠而简便易行的依据。
【】
1 Theilmann L,Klinkert MQ,Gmelin K,et al.Detection of Pre-S1 protein in serum and liver of HbsAg-positive patients: new marker for hepatitis B virus infection. Hepatol, 1986,6:186-190.
2 Neurath AR,kent SB,Strick N,et al.Identification and chemical synthesis of a host cell receptor binding site on hepatitis B virus,Cell,1996,46(3):429.
3 乐爱平.时间分辨免疫荧光技术在检验医学中的现状.江西医学检验,2003,21(3):191-193.
4 秦卫仕,田蓉.时间分辨荧光免疫分析方法学评价.免疫学杂志,2002,18(5):397-405.
5 张言超,寇海兵,朱学文.时间分辨荧光免疫法定量检测HBV标志物的临床意义.齐齐哈尔医学院学报,2003,24(11):1213-1214.











