用DAKO HercepTest检测肝细胞癌HER-2/neu蛋白的表达
作者:冼志红 丛文铭 吴伟清 张秀忠 张树辉
【摘要】 目的 研究肝细胞癌(HCC)中HER-2/neu蛋白的表达及其临床病理意义,探讨应用trastuzumabHCC的可能性。方法 应用DAKO HercepTest抗体,EnVision二步法对868例外科切除病理诊断为HCC标本的HER-2/neu蛋白的表达情况进行观察,并对其与临床病理特征的关系进行统计学分析。结果 868例HCC,有62例(7.14%)出现HER-2/neu 蛋白表达,其中41例大于10%的区域有阳性表达,胞膜显色不连续(1+);20例大于10%的区域有阳性表达,胞膜显色连续,呈局灶强阳性或弥漫中等强度(2+);1例出现70%的瘤细胞弥漫强阳性胞膜阳性(3+)。其余806例无HER-2/neu染色,瘤周肝组织均阴性。 HER-2/neu蛋白表达与HCC的临床病理特征如HBV感染、血清AFP水平、肿瘤大小、组织学分级、胞膜是否完整、有无肝内转移和肝硬化等无明显关系。结论 仅少数HCC(4.84%,42/868)过度表达HER-2/neu蛋白,且与各种临床病理指标无明显相关性,表明其不是HCC的一个重要预后指标,仅个别病例有可能应用抗HER-2/neu单克隆抗体trastuzumab治疗。
【关键词】 肝细胞癌 HER-2/neu 免疫组织化学
Expression of HER-2/neu protein in hepatocellular carcinoma
【Abstract】 Objective To investigate HER-2/neu protein overexpression in hepatocellular carcinoma (HCC),and to explore the possibility of using trastuzumab in treatment of HCC.Methods 868 surgical samples from patients with primary HCC were detected for their HER-2/neu overexpression by DAKO HercepTest,and then the correlations between HER-2/neu overexpression and clinicopathological characteristics were analyzed statistically.Results HER-2/neu immuno-labeling was presented in 62 of 868 cases (7.14%).41 cases showed faint perceptible membrane staining in more than 10% of the neoplastic cells (1+).Strong focal or weak diffuse labeling of more than 10% of the neoplastic cells was presented in 20 cases (2+).1 case showed strong diffuse labeling in more than 70% of the cells (3+).In 806 remaining cases,there was no HER-2/neu labeling.Adjacent benign liver parenchyma was also uniformly negative.All positive controls stained appropriately.No significant relations were observed between HER-2/neu overexpression and clinicopathological parameters.Conclusion HER-2/neu overexpression is detected in 21 (2.42%) of 868 primary HCC cases.Our findings indicates that HER-2/neu overexpression is not an important prognostic factor for patients with HCC.There appears to be no role for usage of anti- HER-2/neu trastuzumab therapy in patients with HCC.
【Key words】 hepatocellular carcinoma HER-2/neu immunohistochemistry
肝细胞癌(hepatocellular carcinoma ,HCC) 是一种常见恶性肿瘤,在我国居恶性肿瘤发病率的第3位,病死率的第2位[1]。因此,寻找敏感而特异的肿瘤标志物对肝癌的早期诊断、治疗方法的合理选择和患者的远期生存率至关重要[2]。研究发现,乳腺癌、卵巢癌、子宫内膜癌、前列腺癌、胃癌等都存在一定比率的HER-2/neu基因扩增,抗HER-2/neu单克隆抗体trastuzumab可有效治疗高表达HER-2/neu的乳腺癌患者[3,4]。但在HCC中HER-2/neu表达的意义仍不完全清楚[5~9],本研究旨在研究HCC中HER-2/neu蛋白的表达及其临床病理意义,探讨应用trastuzumab治疗HCC的可能性。
1 资料与方法
1.1 一般资料 收集第二军医大学东方肝胆外科2002年5月~2003年10月间868例外科切除病理诊断为HCC标本。所有患者术前未经过任何治疗,4μm石蜡切片行HE和AB-PAS染色,组织学诊断按照WHO(2000年)分级标准[10],每例肿瘤的病理诊断由2名病理医师独立完成。本组病例中,男735例,女133例;年龄25~76岁,中位年龄50.3岁;血清AFP≥20μg/L的535例,HBsAg(+)610例;肿瘤直径1~22cm,平均8.9cm;≤3cm 48例,>3cm 820例;高分化26例,中分化798例,低分化44例;844例有肝内转移(包括门脉分支或胆管内癌栓、卫星灶和肝内转移灶);717例伴有肝硬化,其余151例均伴有不同程度的慢性肝炎改变。
1.2 主要试剂 DAKO HercepTest抗体(A0485),购自基因有限公司;EnVision二抗及显色二氨基联苯胺(DAB)为DAKO公司产品。
1.3 染色方法 依据DAKO公司的HercepTest的检测方法,抗体稀释及洗涤液为0.05mol/L,pH 7.4 TBS缓冲液,抗原修复液为0.01mol/L,pH 6.0柠檬酸缓冲液。步骤简述如下:石蜡切片厚度4μm,常规脱蜡至水,微波抗原修复20min,室温冷却,特异性一抗室温(25℃左右)1h,EnVision二抗40min,DAB显色3~5min,以上各步骤之间均用TBS缓冲液浸洗3~5min。自来水终止显色,充分水洗后苏木精对比染色,常规脱水、透明、封片,同时设置阳性、阴性(以TBS代替一抗)对照。
1.4 免疫组织化学结果分析 评分HercepTest的标准及欧美最新的临床实验室标准[11~13]。阳性结果位于肿瘤细胞胞膜,正常肝细胞的细胞质着色或肿瘤组织仅细胞质着色均为非特异染色。评分标准:阴性,无阳性结果表达或非特异着色;1+,大于10%的区域有阳性表达,胞膜显色不连续;2+,大于10%的区域有阳性表达,胞膜显色连续,强度中等;3+,大于10%的区域有阳性表达,胞膜呈连续强阳性表达。对于异质性明显的肿瘤,如同一切片中同时存在1+、2+、3+的情况,以高级别评分。1+为弱阳性,一般无基因扩增,被认为是正常表达,无预后及预测意义;3+为过度表达,一般存在基因扩增,二者符合率达95%,有预测意义;2+为界于两者之间,基因扩增的情况争议较大,特别是DAKO公司多抗的假阳性率高,也包括肿瘤异倍体的情况。
1.5 统计学方法 用SPSS10.0 统计软件包进行分析。HER-2/neu蛋白与其临床病理特征的关系进行Chi-Square检验,以P<0.05表示差异有显著性。
2 结果
HER-2/neu免疫组化结果及其与临床病理的关系,见表1。868例HCC中,有62例(7.14%)出现HER-2/neu 蛋白表达,其中41例大于10%的区域有阳性表达,胞膜显色不连续(见图1);20例大于10%的区域有阳性表达,胞膜显色连续,呈局灶强阳性或弥漫中等强度 (见图2);1例出现70%的瘤细胞弥漫强阳性,胞膜阳性(见图3),患者为29岁女性,肿瘤直径18cm,血清HBsAg(+)、AFP阴性。其余806例无HER-2/neu染色,肿瘤周围肝组织均阴性。HER-2/neu蛋白表达与HCC的临床病理特征如HBV感染、血清AFP水平、肿瘤大小、组织学分级、包膜是否完整、有无肝内转移和肝硬化等无明显关系。
表1 肝细胞癌HER-2/neu蛋白表达及其与临床病理特征的关系 (例)
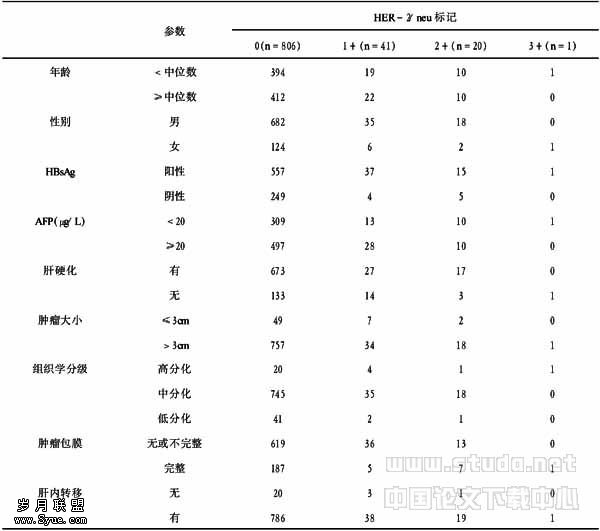
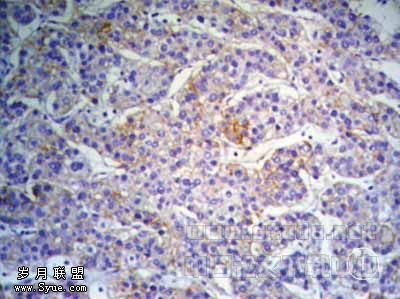
图1 癌细胞胞膜显色不连续(EnVision×200)
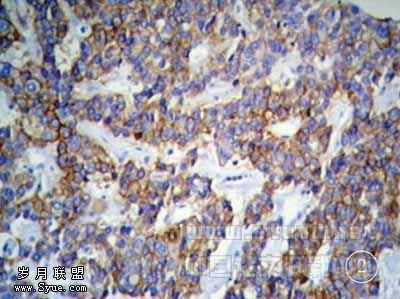
图2 癌细胞胞膜显色连续,强度中等(EnVision×200)
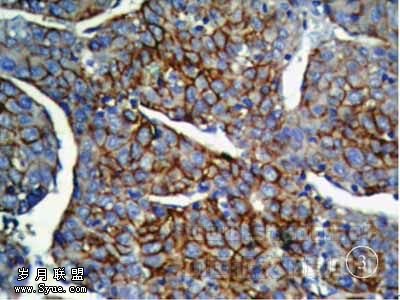
图3 癌细胞胞膜呈连续强阳性表达(EnVision×400)
3 讨论
3.1 HER-2/neu蛋白表达及其与HCC临床病理特征的关系 HER-2/neu也称C-erbB-2,为表皮生长因子受体家族成员之一,是一种原癌基因,该基因定位于人染色体17q21,编码185kD的跨膜糖蛋白(p185)。p185蛋白是由1255个氨基酸组成的酪氨酸激酶受体,在羧基端有自身磷酸化位点。主要在胚胎发育时开始表达,成年后正常组织中可检出少量的HER-2/neu基因,20%~30%的乳腺癌HER-2/neu基因扩增或过表达,卵巢癌、肺癌、胃癌、前列腺癌中也可检出,证明其与这些肿瘤的发生也有一定相关性。HER-2/neu基因表达与乳腺肿瘤的恶性程度有关,良性肿瘤中无表达;低度恶性特殊类型乳腺癌其阳性率低(9?6%);原位癌或浸润性小叶癌中无表达;而高度恶性的浸润性导管癌中其阳性表达率为20%~30%;HER-2/neu基因过度表达的乳腺癌患者中,淋巴结有转移者早期复发,生存率明显降低;淋巴结无转移者亦有早期复发的危险性[3,4,14]。近年Herceptin的研制成功给乳腺癌患者带来了希望,该药已于1998年经美国FDA批准,正式应用于乳腺癌的中,并取得了明显疗效[15]。HCC中HER-2/neu表达的频率从8%升至29?5%[5]。Nakopoulou等[6]应用免疫组化染色显示71例HCC中有21例表达HER-2/neu。Heinze等[7]报道HER-2/neu与HCC的预后相关。但Vlasoff等[8]在HCC、肝细胞腺瘤和正常肝组织中未发现有HER-2/neu过度表达和扩增。Hsu等[9]也发现仅1例巨大HCC伴肺多发转移患者有1+HER-2/neu的表达。本研究用FDA推荐的标准HER-2/neu检测HercepTest试剂盒,显示仅4?84%(42/868)的HCC有HER-2/neu蛋白过度表达,且与各种临床病理指标无明显相关性,表明 HER-2/neu蛋白的过度表达不是HCC的一个重要预后指标,仅个别病例有可能应用抗HER-2/neu单克隆抗体trastuzumab治疗。
3.2 HER-2/neu检测的标准化问题 HER-2/neu基因表达与否,不仅与患者的预后、化疗药物的选择有关,而且与靶向性基因治疗的选择应用有关,故其检测十分重要。目前检测HER-2/neu基因主要有2种方法:一是荧光原位杂交(FISH)测定该基因的扩增与否,另一是免疫组织化学以半定量方式来评估该基因蛋白过表达水平;为美国FDA针对Herceptin治疗乳腺癌而推荐的两种石蜡组织的检测方法。FISH法用于检查17号染色体着丝粒和HER-2/neu基因数量[16,17]。此方法特异性高且敏感,能直接观察HER-2/neu基因的扩增量。阳性者细胞核内出现淡绿色荧光点(染色体着丝粒)。但此项检查价格昂贵,分析结果时计数繁琐,操作复杂,而且需荧光显微镜。免疫组化法是检测HER-2/neu基因蛋白水平较常用的一种方法。它能对HER-2/neu癌基因进行定位,阳性者的细胞膜上出现棕黄色颗粒。此方法简便易行,价格便宜,分析结果时计数方法熟悉,容易掌握,适用于常规福尔马林液固定的石蜡包埋组织,便于进行回顾性研究[18,19]。
用免疫组织化学代替荧光原位杂交方法应该注意几个问题[11~13]:(1) HER-2/neu在肿瘤中的意义是基因扩增并在此基础上的蛋白过度表达,以免疫组织化学来反映基因扩增必须在免疫组织化学结果强阳性的情况下,弱阳性及仅胞质着色属于正常表达,不存在基因扩增,不具有预后及预测意义;(2)需要注意免疫组织化学的假阳性问题。所谓假阳性,是指免疫组织化学检测表达2+以上,但通过FISH等未能检测到基因扩增。已有不少报道DAKO公司HercepTest的假阳性比率高,当然主要存在2+的情况,所以用HercepTest检测HER-2/neu,应该筛选3+的患者用于治疗。免疫组织化学标准化应该从标本固定、抗体试剂的选择、抗原修复技术、结果分析等多方面把关。固定,特别是固定剂的选择和固定时间对免疫组织化学影响较大。笔者认为,由于抗原热修复技术的应用,常规甲醛固定3~4天对抗原影响不大,适合病理科需要延长标本固定的实际情况,但更长时间,如1周以上则抗原性明显减弱。有效的热抗原修复和规范化操作,可使实验可重复性提高。抗体的选择是HER-2/neu免疫组织化学中影响最大的因素。总之,需要特别强调只有对上述检测方法进行统一规范化,才能提供准确的HER-2/neu基因状态,为临床诊断治疗提供可靠的依据。
【】
1 Wu MC,Shen F.Progress in research of liver surgery in China.World J Gastroenterol,2000,6:773-776.
2 Qin LX,Tang ZY.The prognostic molecular markers in hepatocellular carcinoma.World J Gastroenterol,2002,8:385-392.
3 Ross JS,Fletcher JA.Linette GP,et al.The HER-2/neu gene and protein in breast cancer 2003: biomarker and target of therapy.Oncologist,2003,8:307-325.
4 Menard S,Pupa SM,Campiglio M,et al.Biologic and therapeutic role of HER2 in cancer.Oncogene,2003,22:6570-6578.
5 Collier JD,Guo K,Mathew J,et al.C-erbB-2 oncogene expression in hepatocellular carcinoma and cholangiocarcinoma.J Hepatol,1992,14:377-380.
6 Nakopoulou L,Stefanaki K,Filaktopoulos D,et al.C-erbB-2 oncoprotein and epidermal growth factor receptor in human hepatocellular carcinoma: an immunohistochemical study.Histol Histopathol,1994,9:677-682.
7 Heinze T,Jonas S,Karsten A,et al.Determination of the oncogenes p53 and C-erb B2 in the tumour cytosols of advanced hepatocellular carcinoma (HCC) and correlation to survival time.Anticancer Res,1999,19:2501-2503.
8 Vlasoff DM,Baschinsky DY,De Young BR,et al.C-erbB-2 (HER-2/neu) is neither overexpressed nor amplified in hepatic neoplasms.Appl Immunohistochem Mol Morphol,2002,10:237-241.
9 Hsu C,Huang CL,Hsu HC,et al.HER-2/neu overexpression is rare in hepatocellular carcinoma and not predictive of anti-HER-2/neu regulation of cell growth and chemosensitivity.Cancer,2002,94:415-420.
10 Hamilton SR,Aaltonen LA.Pathology and genetics of tumours of the digestive system.IARC Press,2000,165-166.
11 Hammock L,Lewis M,Phillips C,et al.Strong HER-2/neu protein overexpression by immunohistochemistry often does not predict oncogene amplification by fluorescence in situ hybridization.Hum Pathol,2003,34:1043- 1047.
12 Yaziji H,Gown AM.Accuracy and precision in HER-2/neu testing in breast cancer: are we there yet? Hum Pathol,2004,35:143-146.
13 Kobayashi M,Ooi A,Oda Y,et al.Protein overexpression and gene amplification of C-erbB-2 in breast carcinomas:a comparative study of immunohistochemistry and fluorescence in situ hybridization of formalin-fixed,paraffin-embedded tissues.Hum Pathol,2002,33:21-28.
14 Rhodes A,Jasani B,Anderson E,et al.Evaluation of HER-2/neu immunohistochemical assay sensitivity and scoring on formalin-fixed and paraffin-processed cell lines and breast tumors: a comparative study involving results from laboratories in 21 countries.Am J Clin Pathol,2002,118:408-417.
15 Jacobs TW,Gown AM,Yaziji H,et al.Specificity of HercepTest in determining HER-2/neu status of breast cancers using the United States Food and Drug Administration-approved scoring system.J Clin Oncol,1999,17:1983-1987.
16 Lal P,Salazar PA,Hudis CA,et al.HER-2 testing in breast cancer using immunohistochemical analysis and fluorescence in situ hybridization:a single-institution experience of 2,279 cases and comparison of dual-color and single-color scoring.Am J Clin Pathol,2004,121:631-636.
17 Arnould L,Denoux Y,MacGrogan G,et al.Agreement between chromogenic in situ hybridisation (CISH) and FISH in the determination of HER2 status in breast cancer.Br J Cancer,2003,88:1587-1591.
18 Varshney D,Zhou YY,Geller SA,et al.Determination of HER-2 status and chromosome 17 polysomy in breast carcinomas comparing HercepTest and PathVysion FISH assay.Am J Clin Pathol,2004,121:70-77.
19 Hsu CY,Ho DM,Yang CF,et al.Interobserver reproducibility of HER-2/neu protein overexpression in invasive breast carcinoma using the DAKO HercepTest.Am J Clin Pathol,2002,118:693-698.











